Трижды негативный рак молочной железы (ТНРМЖ) — наиболее агрессивный и трудно поддающийся лечению подтип рака груди. Он не реагирует на гормональную терапию и не содержит мишеней для HER2-направленных препаратов, что делает стандартные протоколы менее эффективными.
Однако в последние годы особое внимание привлекает иммунотерапия, способная активировать собственную иммунную систему организма в борьбе с опухолью.
Насколько это эффективно в реальности и кому такая терапия действительно помогает?
Почему именно ТНРМЖ — кандидат на иммунотерапию?
| Критерии для эффективности иммунотерапии | Как проявляется при ТНРМЖ |
|---|---|
| Высокая мутационная нагрузка | У ТНРМЖ часто наблюдается генетическая нестабильность |
| Экспрессия иммунных мишеней (например, PD-L1) | У части пациенток ТНРМЖ обнаруживается PD-L1-позитивный статус |
| Выраженная инфильтрация Т-лимфоцитами (TILs) | ТНРМЖ нередко сопровождается интенсивной иммунной инфильтрацией |
Все это делает его перспективной мишенью для иммунотерапии, особенно ингибиторов контрольных точек (immune checkpoint inhibitors, ICIs).
Кому подойдет иммунотерапия при ТНРМЖ?
| ✅ Показания к иммунотерапии | 🚫 Когда не рекомендуется |
|---|---|
| Неоперабельная или метастатическая форма ТНРМЖ | PD-L1-отрицательная опухоль |
| Подтверждённый PD-L1-позитивный статус | Тяжёлые аутоиммунные заболевания в анамнезе |
| Общее состояние пациента ECOG 0–1 | Быстрое прогрессирование, требующее немедленного эффекта |
| Отсутствие активных иммунопатологий | — |
Ингибиторы PD-1/PD-L1: что действительно работает?
Ингибиторы PD-1 и PD-L1 действуют на сигнальный путь, с помощью которого опухоль «выключает» иммунную систему. Их основная задача — восстановить противоопухолевую активность T-клеток.
Наиболее изученные препараты:
- Пембролизумаб (Keytruda) — PD-1-блокатор, одобрен FDA при ТНРМЖ в комбинации с химиотерапией.
- Атезолизумаб (Tecentriq) — PD-L1-блокатор, использовался в комбинации с наб-паклитакселом.
- Nivolumab (Опдиво) — ингибитор PD-1 (пока off-label для ТНРМЖ)

Что показали крупные исследования:
| 📌 Исследование | Результат | Комментарий |
|---|---|---|
| KEYNOTE-355 (2020) | Пембролизумаб + химиотерапия увеличили PFS до 9.7 мес (против 5.6 мес в контроле) | Ответ сохранялся дольше 1 года у многих PD-L1+ пациенток |
| IMpassion130 (2018) | Атезолизумаб + наб-паклитаксел: общая выживаемость увеличилась до 25 мес (против 15.5 мес) | Только у PD-L1-позитивных пациенток; на основе этих данных было одобрение FDA |
| IMpassion131 (2020) | Эффект отсутствовал | Замена наб-паклитаксела на обычный паклитаксел оказалась неэффективной |
| IMpassion132 (2023) | Также не показало значимого улучшения | Результаты поставили под сомнение эффективность комбинации в других схемах |
| Монотерапия ИКП | Низкая эффективность | Особенно у пациенток с PD-L1-отрицательным статусом |
Тонкости PD-L1-статуса и выбор терапии
PD-L1 — не бинарный маркер. В зависимости от используемого теста (SP142, 22C3, SP263), критерии «позитивности» варьируются:
- CPS ≥ 10 — рекомендован для назначения пембролизумаба (по KEYNOTE-355)
- ≥1% экспрессии PD-L1 на иммунных клетках — использовался в IMpassion130
Разные препараты требуют разной тест-системы, поэтому важно, чтобы диагностика проводилась в опытной лаборатории, а интерпретацией занимался специалист.
Кроме PD-L1 важными становятся:
- TMB (Tumor Mutation Burden) — чем выше мутационная нагрузка, тем выше шанс ответа
- TILs — чем активнее инфильтрация, тем лучше прогноз
- BRCA1/2-статус — влияет на чувствительность к комбинациям с PARP-ингибиторами
Перспективы иммунотерапии при ТНРМЖ: куда движется наука
Иммунотерапия при трижды негативном раке молочной железы активно развивается.
На 2025 год существует более 400 международных клинических исследований, где тестируются новые мишени, комбинации и технологии. Вот ключевые направления, в которых сконцентрированы усилия учёных и клиницистов:
Комбинированные схемы
- Иммунотерапия + химиотерапия — уже стандарт для PD-L1-позитивных форм (например, пембролизумаб + паклитаксел)
- Иммунотерапия + таргетная терапия — изучаются комбинации с PARP-ингибиторами (у BRCA-мутантных пациенток) и AKT-ингибиторами
- Иммунотерапия + антиангиогены — бевацизумаб усиливает иммунную инфильтрацию и делает опухоль более восприимчивой к ИКП
Расширенные checkpoint-комбинации
- PD-1 + CTLA-4 (пембролизумаб + ипилимумаб) — усиленный T-клеточный ответ
- PD-1 + TIGIT или LAG-3 — новые контрольные точки, которые опухоль может использовать для «ухода» от терапии
Персонализированные вакцины и антигены
- Вакцины на основе α-лактальбумина — один из немногих опухолеспецифичных антигенов при ТНРМЖ
- Neoantigen-вакцины — разрабатываются индивидуально, на основе мутационного профиля конкретной опухоли
Клеточные технологии
- TIL-терапия (tumor-infiltrating lymphocytes): лимфоциты, извлечённые из опухоли, активируются вне тела и возвращаются для атаки
- CAR-T и CAR-NK клетки — пока применяются преимущественно при гематологических опухолях, но ведётся адаптация под ТНРМЖ (мишени: GPNMB, mesothelin)
Врожденный иммунитет и иммуноактивация
TLR-активаторы и онколитические вирусы — способствуют разрушению опухоли и повышают чувствительность к иммунотерапии
STING-агонисты — активируют врождённый иммунитет и делают опухоль «видимой» для адаптивной системы
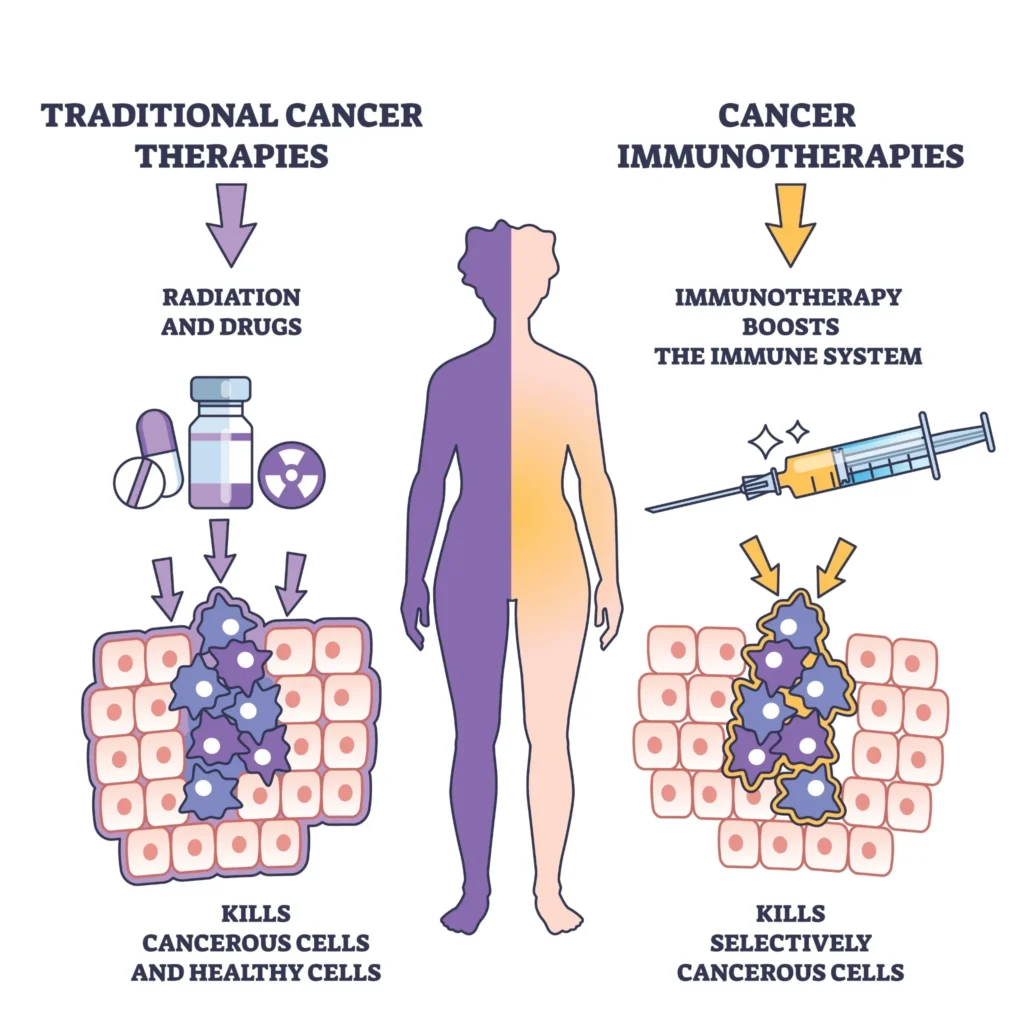
Побочные эффекты: важно знать заранее

Иммунотерапия обладает уникальными побочными эффектами — они связаны не с токсичностью препарата, а с гиперактивацией иммунной системы:
- Аутоиммунный тиреоидит — наиболее частый побочный эффект
- Колиты, гепатиты, пневмониты
- Реже: нейротоксичность, дерматиты, миокардиты
Важно: побочные реакции могут возникнуть спустя месяцы после начала лечения, что требует длительного наблюдения. Многие из них хорошо контролируются глюкокортикоидами, но в тяжёлых случаях терапия отменяется.
Иммуно-мониторинг: как понять, что терапия работает?
Уникальность иммунотерапии — в медленном и нестандартном ответе. Может наблюдаться:
- Псевдопрогрессия — опухоль сначала увеличивается из-за притока лимфоцитов
- Гиперпрогрессия — редкое, но опасное явление — ускорение роста опухоли
- Отсроченный ответ — первые результаты могут быть видны только через 2–4 цикла
Поэтому важно:
- регулярно делать КТ/ПЭТ-КТ по iRECIST-критериям
- сдавать иммунные маркеры (например, IL-6, CD8+ Т-клетки)
- наблюдаться у онколога, знающего особенности оценки иммунного ответа
Микробиом и иммунотерапия: неочевидная связь
Недавние данные показывают: состав микробиома кишечника может влиять на эффективность иммунотерапии. Некоторые бактерии (например, Akkermansia muciniphila) ассоциированы с более сильным ответом на ИКП.
Это открывает новые перспективы:
- Влияние питания и пробиотиков на успех терапии
- Возможность персонализированной коррекции микробиома перед началом курса
Иммунотерапия в Германии: что предлагает европейская медицина
Клиники Германии являются одними из лидеров по применению иммунотерапии при раке молочной железы, включая трижды негативный подтип. Пациентки из других стран могут рассчитывать на:
- Полный онкомолекулярный профиль опухоли (PD-L1, TMB, BRCA, NGS)
- Проведение терапии по международным протоколам (NCCN/ESMO), включая препараты, не всегда доступные в других странах
- Участие в клинических исследованиях фазы II–III для пациенток без стандартных опций лечения
- Мониторинг терапии с применением iRECIST, иммунных биомаркеров и PET-КТ
Важное преимущество — строгие стандарты качества и безопасность, что особенно ценно при назначении препаратов, влияющих на иммунную систему.
Vita Optima сопровождает пациентов на каждом этапе: от сбора документов до выбора клиники, перевода результатов, логистики и постлечебного сопровождения.
Обратитесь в Vita Optima
Если вам или вашим близким поставили диагноз ТНРМЖ и рассматривается иммунотерапия, специалисты Vita Optima помогут организовать лечение в ведущих клиниках Германии, Австрии или Швейцарии.
Мы подберем индивидуальный маршрут, обеспечим доступ к современным методам терапии, консультации ведущих онкологов и полное сопровождение в медицинском путешествии.
Дисклеймер
Информация в статье носит ознакомительный характер и не является медицинской рекомендацией. Для назначения терапии необходима очная консультация онколога и подтверждённый диагноз.